信泰制药「注射用米卡芬净钠」获批上市
4月14日,信泰制药按照老6类申报的抗真菌类药物「注射用米卡芬净钠」的上市申请(CYHS1500411)获国家药品监督管理局批准上市。获批之后,信泰制药是继海正、豪森上海天伟生物和四川制药制剂之后第5家拿到该品种上市资格的国内企业。
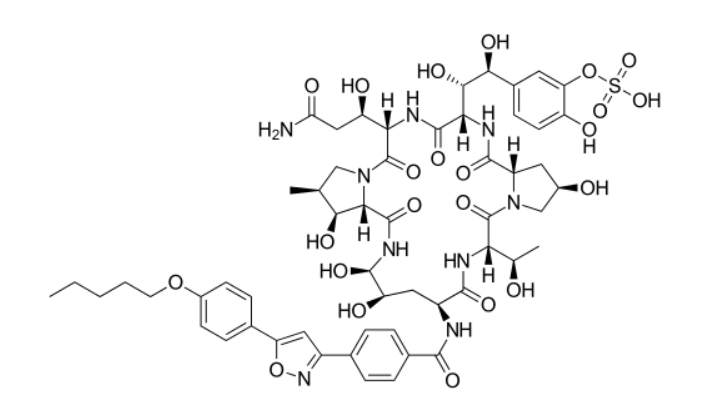
米卡芬净是安斯泰来通过发酵半合成技术开发的脂肽类化合物,也是继卡泊芬净之后获批上市的第二个棘白菌素类抗真菌药物,由真菌Cokeophoma empetri的发酵产物研制而成。
米卡芬净结构式
注射用米卡芬净钠最早于2002年12月在日本上市, 2005年3月通过美国FDA认证,目前仅被批准用于治疗食道念珠菌感染、骨髓移植及ADS患者中性粒细胞减少症的预防治疗。2006年4月即在中国获批,用于治疗由曲霉菌和念珠菌引起的真菌血症、呼吸道真菌病、胃肠道真菌病。 发酵半合成药物,需要先通过发酵技术获得主环粗品,再经过分离纯化获得中间产物,再以中间产物为起始物料,采用合成技术完成侧链拼接,最终获得目标成分。因为“发酵半合成”的产品需要经过发酵,分离纯化,合成等多个技术环节,技术路线和过程参数控制非常复杂。
2018 年,博瑞医药与 Medichem, S.A.签订了《供应与商品化协议》约定博瑞医药向Medichem, S.A.供应米卡芬净钠中间体,博瑞医药从Medichem, S.A. 的对外销售的利润中获取分成。
海正药业是国内发酵半合成技术的领先企业之一,在2018/4/12获批拿下注射用米卡芬净钠首仿;豪森则紧随其后在2018/5/23获批上市,后两者分别通过一致性评价。另外,目前该品种还有杭州中美华东、扬子江药业、奥赛康3家企业申报上市,其中扬子江药业按照新4类申报上市,一旦获批将视同通过一致性评价。
- 欧洲药品管理局受理安斯泰来Zolbetu
东京,2023年7月13日 -- 安斯泰来制药集团(TSE:...
- 暴增650.92%!哈药做对了什么?
疫情后,中药、OTC、保健品销售率先走向复苏,其中“老字号”...
- 新政赋能,力扬企业扬帆助推中医药科技发展
最近,国务院办公厅正式印发 《中医药振兴发展重大工程实施方案...
- 医药之家:多款1类新药相继获批上市!
随着国家创新发展战略的实施,近几年,中国制药业的创新成果正逐...